- Funktion der Blutplättchen (Thrombozyten) bei der Eigenbluttherapie
- Was macht das Blutplasma?
- Was ist autologes plättchenreiches Plasma (A-PRP)?
- Anwendungsgebiete der Eigenbluttherapie mit A-PRP
- A-PRP zur Behandlung von Arthrose
- Sportverletzungen mit plättchenreichem Plasma (A-PRP) behandeln
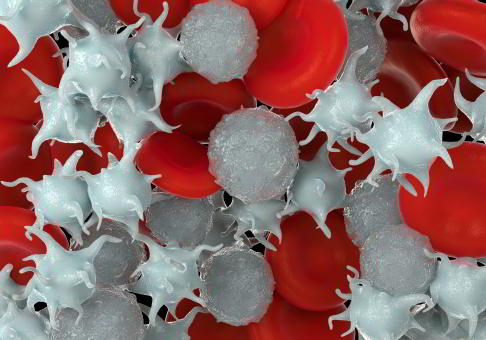 Wenn Thrombozyten aktiviert sind, bilden sie kleine Tentakeln aus. Diese helfen ihnen, an der Wunde haften zu bleiben und zu verklumpen. Auf diese Weise verschließen sie die Verletzung. Neben der Bildung von mechanischen Barrieren zur Blutstillung nach Verletzung haben Thromobozyten (Blutplättlichen) auch umfassende biochemische Fähigkeiten: Sie bilden Wachstumsfaktoren, stimulieren die Gewebsregeneration an Verletzungsorten und senken die Entzündungsneigung. Hormone aus Thrombozyten fördern die Ausbildung von Bindegewebe und der Zelldifferenzierung und Wachstum zur Regeneration von geschädigtem Gewebe. Diese natürlichen Eigenschaften werden im Rahmen von Eigenbluttherapie zunehmend auch medizinisch z. B. bei der Therapie von Arthrose oder bei Sportverletzungen genutzt. © royaltystockphoto, stock.adobe.com
Wenn Thrombozyten aktiviert sind, bilden sie kleine Tentakeln aus. Diese helfen ihnen, an der Wunde haften zu bleiben und zu verklumpen. Auf diese Weise verschließen sie die Verletzung. Neben der Bildung von mechanischen Barrieren zur Blutstillung nach Verletzung haben Thromobozyten (Blutplättlichen) auch umfassende biochemische Fähigkeiten: Sie bilden Wachstumsfaktoren, stimulieren die Gewebsregeneration an Verletzungsorten und senken die Entzündungsneigung. Hormone aus Thrombozyten fördern die Ausbildung von Bindegewebe und der Zelldifferenzierung und Wachstum zur Regeneration von geschädigtem Gewebe. Diese natürlichen Eigenschaften werden im Rahmen von Eigenbluttherapie zunehmend auch medizinisch z. B. bei der Therapie von Arthrose oder bei Sportverletzungen genutzt. © royaltystockphoto, stock.adobe.com
Die Behandlung von Krankheiten und Verletzungen mit körpereigenen Substanzen aus dem Blut ist in der Medizin schon seit Jahren etabliert. Bereits im 19. Jahrhundert wurden erste Eigenbluttherapien zur Behandlung von Infektionskrankheiten durchgeführt. Bei Eigenbluttherapien wird dem Patienten stets eine kleine Menge des eigenen Blutes aus der Armvene abgenommen, verarbeitet und konzentriert in das Gelenk mit Arthrose oder eine entzündete Sehne injiziert. Die Behandlung mit autologem plättchenreichen Plasma (A-PRP), bei der vor allem die Blutplättchen verarbeitet werden, ist eine spezifische Form der Eigenbluttherapie.
Ende des 20. Jahrhunderts kam es zu ersten Herstellungsversuchen von plättchenreichem Plasma aus zentrifugiertem Eigenblut. Heute wird die Eigenbluttherapie zur Behandlung offener Wunden sowie in der Herz-/Thorax-, Zahn- und plastischen Chirurgie eingesetzt. Ein weiteres Anwendungsgebiet ist die Orthopädie. Vor allem bei Knorpelschäden (Arthrose), Sehnen- oder Bandverletzungen, Muskelzerrungen und Entzündungen verschiedener Weichteilgewebe, z. B. Schleimbeutel (Bursitis) oder Sehnenscheidenentzündungen (Tendinitis) hat sich die Methode in der Praxis bewährt.
Funktion der Blutplättchen (Thrombozyten) in der Eigenbluttherapie
Die Blutplättchen (Thrombozyten) werden im Knochenmark gebildet und sind für die Blutgerinnung (Hämostase) zuständig. Dieser lebenswichtige Reparaturmechanismus, an dem neben den Blutplättchen noch weitere Faktoren beteiligt sind, verschließt blutende Wunden. Bei gesunden Menschen befinden sich in einem Mikroliter (1 Mikroliter = 0,1 ml) Blut etwa 150.000 bis 380.000 Thrombozyten. Wurde ein Blutgefäß im Körper verletzt, lagern sich die Blutplättchen an der Stelle an und verklumpen. Dieser Blutpfropfen verschließt die Wunde und stillt die Blutung. Die Thrombozyten schütten hormonähnliche Wachstumsfaktoren aus, die den Heilungsprozess fördern. Zudem ziehen sie Stammzellen an, die sich zu verschiedenen Gewebetypen differenzieren können. Diese Stammzellen benötigt der Körper zur Regeneration von geschädigtem Gewebe.
Was ist die Rolle des Blutplasmas?
Als Blutplasma bezeichnet man den flüssigen Anteil des Blutes, der etwa 55 % des Gesamtvolumens ausmacht. Seine Aufgabe ist der Transport der Blutzellen und Nährstoffe durch das Gefäßsystem. Neben dem Blutplasma besteht das Blut aus zellulären Bestandteilen, dem sogenannten Hämatokrit. Dazu zählen vor allem die roten Blutkörperchen (Erythrozyten), die mit etwa 99 % den Hauptbestandteil des Hämatokrits ausmachen und für den Sauerstofftransport verantwortlich sind. Weitere zelluläre Bestandteile des Blutes sind die weißen Blutkörperchen (Leukozyten), die für die Immunabwehr zuständig sind und die für die Blutgerinnung wichtigen Blutplättchen (Thrombozyten). Je höher der Hämatokritwert ist, desto zähflüssiger ist das Blut. Dies kann z. B. auf einen Flüssigkeitsmangel hinweisen. Ist hingegen der Anteil des Blutplasmas erhöht, kann dies ein Hinweis auf einen Mangel an Erythrozyten sein. Man spricht dann von einer Anämie (Blutarmut).
Was ist autologes plättchenreiches Plasma (A-PRP)?
Autologes plättchenreiches Plasma (A-PRP) ist ein aus dem Patientenblut gewonnenes Thrombozytenkonzentrat. Es besteht aus Blutplasma, aus dem rote und weiße Blutkörperchen zu einem Großteil herausgefiltert wurden.
Für die Herstellung des körpereigenen plättchenreichen Plasmas entnimmt man dem Patienten mit einer Spritze etwa 10 bis 60 ml Blut aus dem Arm. Das Blut wird dann zentrifugiert, um das Plasma von den zellulären Bestandteilen abzutrennen. Diesen Prozess nennt man Plasmapherese. Das Verfahren wendet man auch zur Vorbereitung der Eigenbluttherapie an. Damit das Blut nicht gerinnt, wird es mit dem Gerinnungshemmer Citrat (Zitronensäure) versetzt.
In einem weiteren mehrphasigen Prozess wird das Blutplasma mit den körpereigenen Blutplättchen (Thrombozyten) angereichert. Auf diese Weise erreicht man eine drei- bis sechsmal höhere Konzentration der für die Wundheilung wichtigen Thrombozyten. Das plättchenreiche Plasma (engl: “platelet rich plasma”, kurz: PRP) unterstützt lokal, also dort wo man es wieder in den Körper injiziert, körpereigene Heilungsprozesse und trägt zur Regeneration von Gewebe (z. B. Knorpel) bei. Der genaue Wirkmechanismus der Therapiemethode ist allerdings bislang nicht geklärt. Man vermutet, dass die im Blutplasma angereicherten Wirkstoffe (z. B. sog. Interleukine, Thrombozyten) den Heilungsprozess im entzündeten Gewebe (Sehnen, Knorpel) anregen und unterstützen. Es ist lediglich bekannt, dass die Thrombozyten die Bildung von Bindegwebe stimulieren, Entzündungen hemmen und über mehrere biochemische Wirkketten gleichzeitig eine potentiell knorpelschützende Wirkung entfalten.
Da die Zusammensetzung dieser Wirkstoffe des Blutes und das innere Milieu von Patient zu Patient variiert, kann es zu unterschiedlichen Ergebnissen nach der Behandlung mit autologem plättchenreichem Plasma kommen. Nebenwirkungen wie Immunabwehr oder Allergien können nicht hervorgerufen werden, da es sich um eine körpereigene Substanz des Patienten handelt.
Die Behandlungskosten für die Therapie mit A-PRP werden von einigen privaten Krankenkassen übernommen. Die gesetzlichen Kassen zahlen die Behandlung bisher nicht.
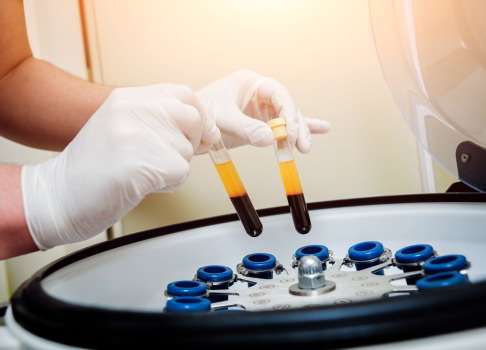 Das für die Eigenbluttherapie notwendige Blut wird in einer Zentrifuge weiterverarbeitet. Dabei werden die zellulären Bestandteile und das Plasma voneinander separiert. Die für die Wundheilung und Regeneration notwendigen Thrombozyten können so angereichert und für eine Injektion in Gelenke mit Arthrose oder entzündete Sehnen weiterverarbeitet werden. © romaset, Fotolia
Das für die Eigenbluttherapie notwendige Blut wird in einer Zentrifuge weiterverarbeitet. Dabei werden die zellulären Bestandteile und das Plasma voneinander separiert. Die für die Wundheilung und Regeneration notwendigen Thrombozyten können so angereichert und für eine Injektion in Gelenke mit Arthrose oder entzündete Sehnen weiterverarbeitet werden. © romaset, Fotolia
Anwendungsgebiete der Eigenbluttherapie mit A-PRP
Die Therapie mit A-PRP kommt bei folgenden Erkrankungen des Bewegungsapparates zum Einsatz:
- Arthrose (Gelenkverschleiß) und Arthritis (Gelenkentzündung)
- Entzündung von Weichteilgewebe (z. B. Sehnenscheidenentzündung)
- Muskelzerrungen und Muskelfaserrisse
- Bänderrisse und -teilrisse
- Sehnenentzündungen (z. B. Achillodynie)
- Bandscheibenvorfälle
- Verletzung der Rotatorenmanschette des Schultergelenks
- Unterstützung der Wundheilung bei Operationen (z. B. Arthroskopie)
Die Anwendungsgebiete der Eigenbluttherapie mittels autologem (körpereigenem) plättchenreichen Plasma sind in der Medizin vielfältig. Es kommt beispielsweise in der Zahnmedizin oder Herzchirurgie zur Verbesserung der Wundheilung bei einem operativen Eingriff zum Einsatz. In der Orthopädie verwendet man das körpereigene Thrombozytenkonzentrat vor allem zur Behandlung von Knorpelschäden, Sehnenentzündungen oder Sportverletzungen. Indikationen sind unter anderem Arthrosen in Knie, Fuß oder Sprunggelenk sowie Reizsyndrome und Risse (Rupturen) der Achillessehne und anderer Sehnen. Auch bei Verletzung der Muskeln und Bänder (z. B. Kreuzband oder Rotatorenmanschette) kann die Eigenbluttherapie mit autologem PRP die Heilung und Regeneration unterstützen.
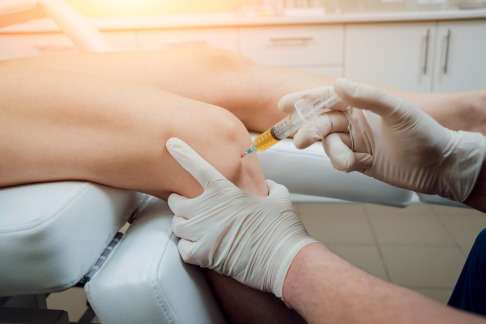 Injektion eines Eigenblutpräparates in das Kniegelenk mit Arthrose. Autologes plättchenreiches Plasma unterstützt den Körper bei der Wundheilung und eignet sich daher für die Behandlung von Sportverletzungen wie Muskelzerrungen oder Schleimbeutelentzündungen. © romaset, stock.adobe.com
Injektion eines Eigenblutpräparates in das Kniegelenk mit Arthrose. Autologes plättchenreiches Plasma unterstützt den Körper bei der Wundheilung und eignet sich daher für die Behandlung von Sportverletzungen wie Muskelzerrungen oder Schleimbeutelentzündungen. © romaset, stock.adobe.com
A-PRP zur Eigenblut-Behandlung von Arthrose
Die Arthrose ist eine Gelenkerkrankung, die mit dem Verschleiß des Gelenkknorpels einhergeht. Da durch den zunehmenden Knorpelabrieb die puffernde und schützende Funktion des Knorpels verlorengeht, reiben bei fortgeschrittener Arthrose die knöchernen Gelenkpartner zunehmend aufeinander. So kommt es zu Schmerzen und Bewegungseinschränkungen im betroffenen Gelenk. Die am häufigsten betroffenen Gelenke sind Knie und Hüfte, die das gesamte Körpergewicht tragen.
Alternativen zur Eigenbluttherapie bei Arthrose
Zur konservativen Behandlung der Arthrose werden neben entlastenden Orthesen oder Krankengymnastik auch pharmakologische Substanzen wie entzündungshemmende Schmerzmittel (z. B. Ibuprofen), Hyaluronsäure oder Kortison eingesetzt.
Erfahrungen mit der Eigenbluttherapie
Auch die Behandlung der Arthrose mit körpereigenem plättchenreichen Plasma wird seit einiger Zeit in der Praxis durchgeführt und erzielt überzeugende Ergebnisse. Vor allem das Auftreten entzündlich aktivierter Arthrose, die mit Schwellung und Überwärmung des Gelenkes einhergeht, wird durch das A-PRP-Verfahren vermindert. Die Entzündungsneigung des Gelenks geht nach Injektion häufig deutlich zurück. Da das Verfahren noch relativ neu ist, fehlen allerdings Langzeitstudien.
Warum ist Eigenbluttherapie eine Alternative zu anderen Arthrosetherapien?
Das autologe (körpereigene) PRP soll die Schmerzen lindern und die Beweglichkeit des Gelenks wiederherstellen. Dafür wird das plättchenreiche Plasma aus dem Vollblut des Patienten gewonnen. Der Orthopäde spritzt das Thrombozytenkonzentrat direkt ins betroffene Gelenk, wo es die Knorpelregeneration anregen soll. In der Regel sind mehrere Anwendungen der A-PRP-Injektion erforderlich, damit sich eine Wirkung einstellen kann.
Dabei haben Studien gezeigt, dass die A-PRP-Injektion bei Kniearthrose über 12 Monate deutlich besser schmerzlindernd wirkte als eine Plazebo-Injektion mit Kochsalzlösung (Görmeli et al, 2014).
Weil die bei aktivierter Arthrose verbreitete Kortisoninjektion gewebeschädigend sein kann und zur Atrophie (Rückbildung) von Bindegewebe führt, stellt die Behandlung mit A-PRP im Vergleich dazu einen schonenden Ansatz zur Regulierung von Entzündungen dar.
Anders als nichtsteroidale Antirheumatika hat A-PRP kein Potential zu schweren Nebenwirkungen z. B. auf den Verdauungstrakt.
In verschiedenen Studien wurde auch gezeigt, dass A-PRP-Injektion einer der Hyaluronsäureinjektion bei Kniearthrose vergleichbare oder meist sogar überlegene klinische Wirkung hat.
Das plättchenreiche Plasma hat verschiedene nachweisbare Wirkungen auf das Knorpelgewebe (Cook et al, 2018), die gemeinsam einen knorpelschützenden und knorpelaufbauenden Effekt haben können:
- Wachstumsfaktoren werden von den Blutplättchen ausgeschüttet: Sie stimulieren das Wachstum (Proliferation) der Knorpelzellen.
- Gerinnungsfaktoren und Cytokine der Blutplättchen stimulieren die knorpelbildende (chondrogene) Aktivität der Knorpelzellen.
- Gerinnungsfaktoren hemmen (inhibieren) die knorpelabbauende Wirkung von Entzündungsmediatoren.
- Wachstumsfaktoren, die von Blutplättchen sekretiert werden, enthalten TGF-β, IGF-1, BMP, PDGF, VEGF als wichtige Faktoren zur Beschleunigung von Wachstum und Ausdifferenzierung von Knorpelzellen sowie zur Wiederherstellung der Nährstoffzufuhr zu den damit behandelten Geweben.
- Bildung von Typ II Kollagen als wichtiger Bestandteil des Knorpelgewebes wird gefördert.
- Entzündungen bei entzündlich aktivierter Arthrose wird beendet.
- Förderung der Bildung des in der Gelenkflüssigkeit reichlich vorhandenen knorpelstabilisierenden Proteins Lubricin (Proteoglykan 4).
Auch im Vergleich zur Hyaluronsäure-Injektion ist die Therapie mit A-PRP die effektivere Methode. Bei Patienten mit einer beginnenden Arthrose konnte die Schmerz- und Bewegungssituation des betroffenen Gelenkes signifikant verbessert werden.
Wissenschaftliche Beurteilung der A-PRP-Therapie bei Arthrose:
Es gibt mehrere Faktoren, die die Entwicklung von Arthrose beinflussen. Dazu gehört die Inhibition (Hemmung) von entzündungsfördernden Cytokinen in der Gelenkflüssigkeit. A-PRP-Therapie soll die entzündungsfördernden Stoffwechselfaktoren in der den knorpel abbauenden Umgebung des Gelenks moderieren. Es gibt eine zunehmende Anzahl von Studien, die zeigen, dass eine Behandlung mit A-PRP bei der nichtoperativen Therapie der Gelenkarthrose einen klinischen Vorteil bietet (Cook et al, 2018).
Zusätzliche randomisierte und kontrollierte Langzeit-Studien sind erforderlich, um die therapeutische Effizienz der Eigenbluttherapie mit A-PRP bei Arthrose abschließend bewerten zu können. Weitere präklinische Studien sollen die Effizienz und den Wirkmechanismus der A-PRP-Therapie in der klinischen Anwendung der Arthrosebehandlung molekularbiologisch genau zeigen. (Mitchell et al, 2018).
 Autologes plättchenreiches Plasma unterstützt den Körper bei der Wundheilung und eignet sich daher für die Behandlung von Sportverletzungen wie Muskelzerrungen, Sehnenentzündungen oder Schleimbeutelentzündungen. © massimhokuto, stock.adobe.com
Autologes plättchenreiches Plasma unterstützt den Körper bei der Wundheilung und eignet sich daher für die Behandlung von Sportverletzungen wie Muskelzerrungen, Sehnenentzündungen oder Schleimbeutelentzündungen. © massimhokuto, stock.adobe.com
Sportverletzungen und Sehnenentzündungen mit plättchenreichem Plasma (A-PRP) behandeln
Vor allem bei Kontaktsportarten wie Fußball oder Hockey kommt es häufig zu mechanischen Verletzungen an Muskeln, Knorpeln, Sehnen oder Bändern. Aber auch durch chronische Überlastung oder Fehlbelastung kann es zu Verletzungen kommen. Hier sind vor allem Sehnenreizungen (z. B. Tennisarm) oder Entzündungen von Weichteilen wie Schleimbeuteln (Bursae) oder Sehnenscheiden zu nennen.
Autologes plättchenreiches Plasma bietet bei der Therapie von Sportverletzungen eine Alternative zu herkömmlichen Behandlungsmethoden. Die Injektion des körpereigenen Thrombozytenkonzentrats wirkt entzündungshemmend und lindert Schmerzen. Durch die enthaltenen Wachstumsfaktoren unterstützt es den Körper bei der Wundheilung und fördert die Regeneration des geschädigten Gewebes.